:format(jpg)/f.elconfidencial.com%2Foriginal%2F77e%2Fbf2%2Fa41%2F77ebf2a416ba68b3848543fe9d1d1b44.jpg)
¿Qué es el medicamento Ala Octa? Para qué se usaba y qué efectos adversos tiene
La Fiscalía de la Audiencia Nacional acaba de presentar querella contra las empresas alemanas Alamedics GmbH & Co.KG y BSI Group Deutschland, y la empresa con sede en Barcelona W.M. Bloss SA, por la fabricación, evaluación y comercialización, respectivamente, del producto sanitario defectuoso Ala Octa (Perfluoroctano), causante de efectos adversos a la salud de ciudadanos españoles usuarios de los servicios sanitarios. En concreto, se han identificado varios casos de ceguera.
El Ministerio Público considera que los hechos pueden encajar en delitos contra la salud pública y de lesiones graves. El producto Ala Octa a base de perfluoroctano (C8F18) se utilizaba como coadyuvante intraoperatorio en cirugías oftálmicas, por ejemplo, en los desprendimientos de retina. El producto ocasionó a los pacientes a quienes se les suministró “efectos adversos para la salud como amaurosis (situación de no percepción de luz en el ojo operado), atrofia del nervio óptico (atrofia óptica), necrosis retiniana y fenómenos de oclusión vascular retiniana con posible envainamiento de la pared de los vasos sanguíneos de la retina, tanto arteriales como venosos”, informa el departamento. La investigación sobre el producto apreció la existencia de deficiencias en la fabricación y carencias en los controles de seguridad de la materia prima y de los lotes fabricados. Fue utilizado por el sistema de salud español en 28 centros sanitarios, de 13 comunidades autónomas, con un número total de 125 casos notificados.
La decisión se adopta después de que el Ministerio Público arrancara hace unos meses unas diligencias preprocesales para determinar si existían responsabilidades sanitarias en los casos de pacientes a quienes, con motivo de cirugía de retina, se les fue suministrado el producto. Las diligencias se incoaron con motivo de una denuncia presentada por la asociación El Defensor del Paciente, exponiendo la situación de indefensión y desprotección en la que se encuentran los usuarios-pacientes de los servicios sanitarios, a quienes se les aplicó este tratamiento en las intervenciones de retina causándoles pérdida de visión.
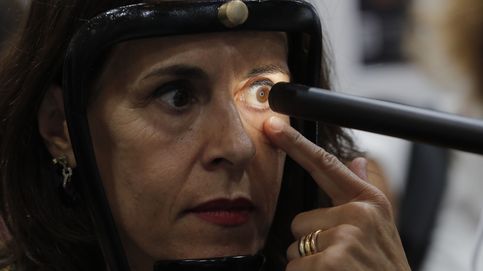
¿Qué es el medicamento Ala Octa? Para qué se usaba y qué efectos adversos tiene
El Confidencial
La Agencia Española de Medicamentos y Productos Sanitarios (Aemps) ordenó retirar del mercado el producto, un compuesto sintético de carbono y flúor fabricado por una empresa alemana, Ala Medics GmbH, y de uso común en intervenciones oftalmológicas y utilizado con frecuencia en cirugías de retina. Los ensayos realizados confirmaron su toxicidad. El fabricante alemán Ala Medics lo comercializó en el mercado español por el distribuidor español WM Bloss.
Alertas sanitarias
La Agencia Española de Medicamentos emitió la primera alerta sanitaria advirtiendo sobre el carácter defectuoso de dicho producto en junio de 2015, con posteridad a su utilización por parte de distintos servicios de salud, entre ellos el de Castilla y León. El producto sanitario había obtenido el sello o marchamo CE, otorgado por el Organismo Notificado BSI Group, por lo que, de acuerdo la normativa comunitaria, dicho producto sanitario podía circular libremente en la Unión Europea.
Según específica la querella, el fiscal reclama recabar de los centros sanitarios que notificaron incidentes información de los pacientes que sufrieron lesiones, que se les cite con ofrecimiento de acciones y examen médico forense para determinar la entidad, el momento en que se produjo la lesión, que se requiera el organigrama de las farmacéuticas para determinar las personas físicas que pudieran resultar responsables, se las cite como imputadas y que se aseguren las responsabilidades civiles en vista a compensar a los afectados.
{getToc} $title={Tabla de Contenidos}
